国家药监局官网发布《2021年度药品审评报告》。
报告明确:2021年审评通过47个创新药,再创历史新高,临床急需境外新药上市持续加快,优先审评效率大幅提高,仿制药质量和疗效一致性评价工作扎实推进,临床试验管理跃上新台阶,核查检验协调机制更加通畅,实施药品电子通用技术文档申报,中国上市药品专利信息登记平台建设运行,完成中药“三方”抗疫成果转化,完善符合中医药特点的审评技术标准体系,支持和推动中药传承创新发展,持续深化ICH工作,保障国家药品监督管理局成功连任ICH管理委员会成员,发布87个技术指导原则,审评标准体系更加完备,流程导向审评体系更加科学,审评体系和审评能力现代化建设持续推进,医药产业创新能力和高质量发展进一步增强。
2021年是党和国家历史上具有里程碑意义的一年。以习近平同志为核心的党中央团结带领全党全国各族人民,隆重庆祝中国共产党成立一百周年,胜利召开党的十九届六中全会、制定党的第三个历史决议,如期打赢脱贫攻坚战,如期全面建成小康社会、实现第一个百年奋斗目标,开启全面建设社会主义现代化国家、向第二个百年奋斗目标进军新征程。在“十四五”开局之年,作为我国负责药品注册上市的专职技术审评机构,国家药品监督管理局药品审评中心(以下简称药审中心)始终坚决贯彻落实习近平总书记重要讲话和重要指示精神,全面践行“四个最严”要求,牢记保护和促进公众健康初心使命,坚持人民至上、生命至上和科学审评,积极投身药品审评审批制度改革事业,紧紧围绕人民生命健康、世界科技前沿、国家重大需求等战略目标,在体制机制、技术标准、流程管理、队伍建设等方面加快创新融合步伐。
面对复杂严峻的疫情防控形势和极为艰巨繁重的药品审评任务,药审中心在国家药品监督管理局党组的坚强领导下,以习近平新时代中国特色社会主义思想为指导,深入学习贯彻党的十九届五中、六中全会精神和“七一”重要讲话精神,认真落实党中央、国务院决策部署,推动全面从严治党不断向纵深发展,认真开展好党史学习教育和“我为群众办实事”实践活动,全力推进新冠病毒疫苗药物应急审评审批,推动2款国产新冠病毒疫苗接连被纳入世界卫生组织(WHO)紧急使用清单(EUL),应急审评通过一组新冠病毒中和抗体联合治疗药物上市,着力建设公开透明的审评机制,多措并举支持儿童用药研发创新,人民获得感、幸福感、安全感显著增强。
2021年审评通过47个创新药,再创历史新高,临床急需境外新药上市持续加快,优先审评效率大幅提高,仿制药质量和疗效一致性评价工作扎实推进,临床试验管理跃上新台阶,核查检验协调机制更加通畅,实施药品电子通用技术文档申报,中国上市药品专利信息登记平台建设运行,完成中药“三方”抗疫成果转化,完善符合中医药特点的审评技术标准体系,支持和推动中药传承创新发展,持续深化ICH工作,保障国家药品监督管理局成功连任ICH管理委员会成员,发布87个技术指导原则,审评标准体系更加完备,流程导向审评体系更加科学,审评体系和审评能力现代化建设持续推进,医药产业创新能力和高质量发展进一步增强。
第一章 药品注册申请受理情况
(一)总体情况
1.全年受理情况
2021年,国家药品监督管理局药品审评中心(以下简称药审中心)受理注册申请11658件1,同比增长13.79%。
受理需技术审评的注册申请9235件,同比增长29.11%,包括需经技术审评后报送国家局2审批(以下简称技术审评)的注册申请2180件,需经技术审评后以国家局名义作出行政审批(以下简称审评审批)的注册申请7051件,需经技术审评后送国家药品监督管理局医疗器械技术审评中心、以医疗器械作用为主的药械组合(以下简称药械组合)产品的注册申请4件。
受理无需技术审评直接以国家局名义作出行政审批3(以下简称直接审批)的注册申请2423件。2017-2021年注册申请受理量详见图1。
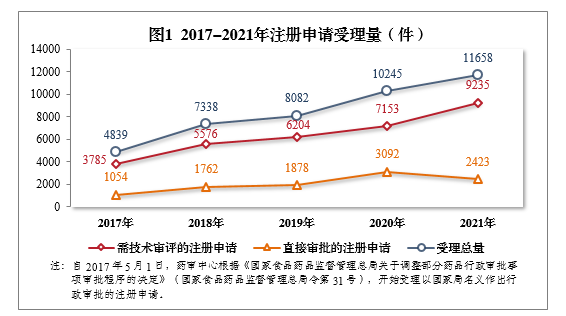
根据《国家药监局关于进一步完善药品关联审评审批和监管工作有关事宜的公告》(2019年第56号,以下简称56号公告)要求,2021年受理原料药注册申请1313件,同比增长2.98%。
2.需技术审评的各类注册申请受理情况
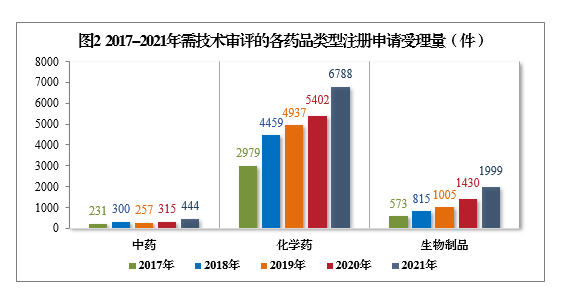
2021年受理的需技术审评的9231件4注册申请中,以药品类型统计,中药5注册申请444件,同比增长40.95%;化学药注册申请为6788件,同比增长25.66%,占全部需技术审评的注册申请受理量的73.53%;生物制品注册申请1999件,同比增长39.79%。2017-2021年需技术审评的各药品类型注册申请受理量详见图2。
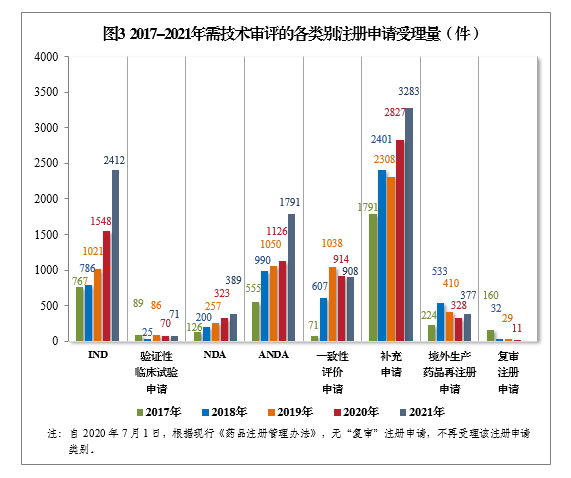
以注册申请类别统计,受理新药临床试验申请(该注册申请类别以下简称IND)2412件,同比增长55.81%;新药上市许可申请(该注册申请类别以下简称NDA)389件,同比增长20.43%;同名同方药、仿制药、生物类似药上市许可申请(该注册申请类别以下简称ANDA)1791件,同比增长59.06%;仿制药质量和疗效一致性评价注册申请6(该注册申请类别以下简称一致性评价申请)908件;补充申请3283件,同比增长16.13%。2017-2021年需技术审评的各类别注册申请受理量详见图3。
(二)创新药注册申请受理情况
2021年受理创新药7注册申请1886件(998个品种8),同比增长76.10%。
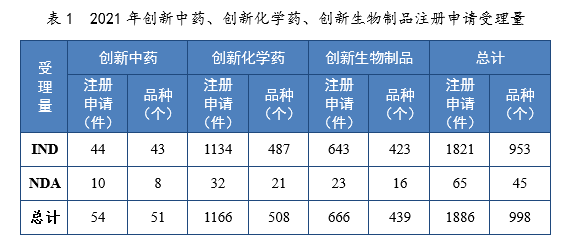
以药品类型统计,创新中药54件(51个品种),同比增长134.78%;创新化学药1166件(508个品种),同比增长55.05%;创新生物制品666件(439个品种),同比增长125.00%。
以注册申请类别统计,IND 1821件(953个品种),同比增长79.23%;NDA 65件(45个品种),同比增长18.18%。
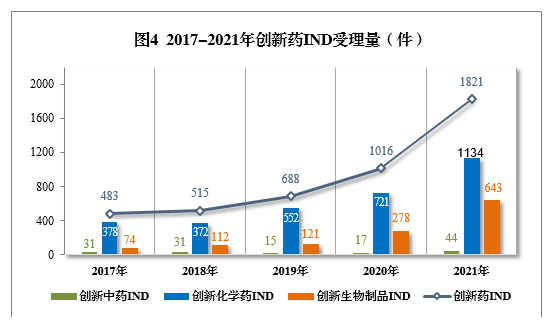
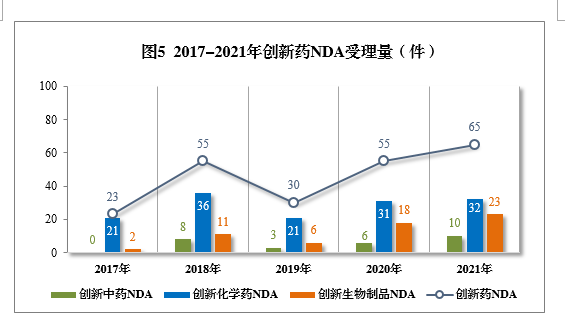
2021年创新中药、创新化学药、创新生物制品注册申请受理量详见表1,2017-2021年创新药IND受理量详见图4,2017-2021年创新药NDA受理量详见图5。
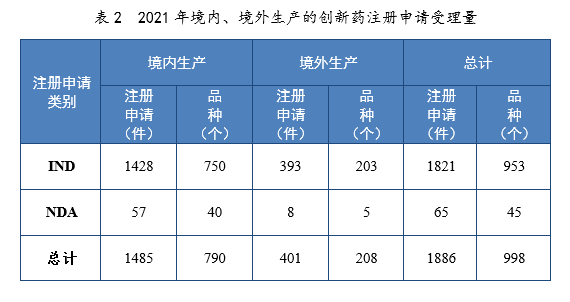
以生产场地类别统计,境内生产创新药1485件(790个品种),境外生产创新药401件(208个品种)。2021年境内、境外生产的创新药注册申请受理量详见表2。
(三)需技术审评的中药注册申请受理情况
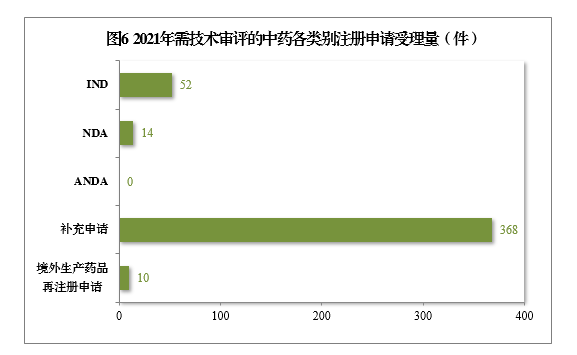
2021年受理需技术审评的中药注册申请444件。以注册申请类别统计,IND 52件,同比增长136.36%,包括创新中药IND 44件(43个品种),同比增长158.82%;NDA 14件,同比增长133.33%,包括创新中药NDA 10件(8个品种),同比增长66.67%。
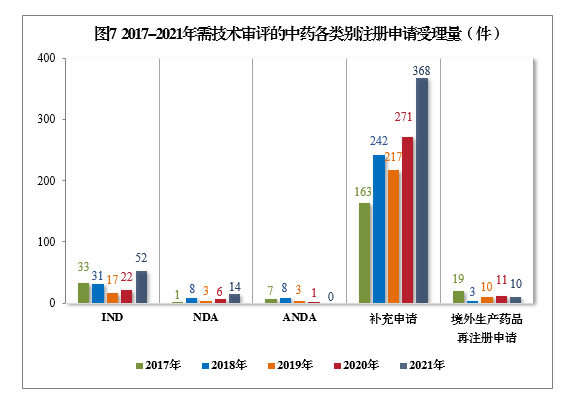
2021年需技术审评的中药各类别注册申请受理量详见图6。2017-2021年需技术审评的中药各类别注册申请受理量详见图7。
(四)需技术审评的化学药注册申请受理情况
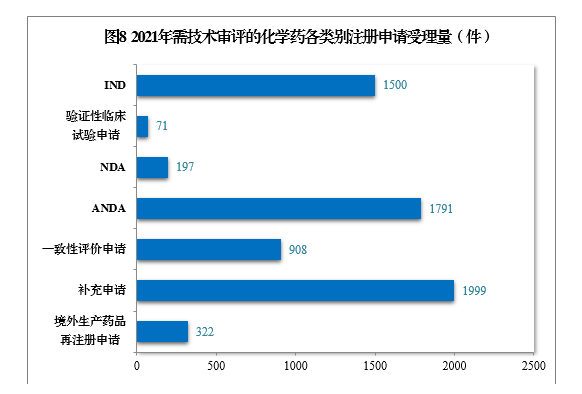
2021年受理需技术审评的化学药注册申请6788件。以注册申请类别统计,IND 1500件,同比增长58.56%,包括创新化学药IND 1134件(487个品种),同比增长57.28%;NDA 197件,同比增长3.14%,包括创新化学药NDA 32件(21个品种),同比增长3.23%;化学药5.1类9注册申请169件,同比增长5.63%,其中临床试验申请10共44件,NDA 125件;ANDA 1791件,同比增长59.20%;一致性评价申请908件。
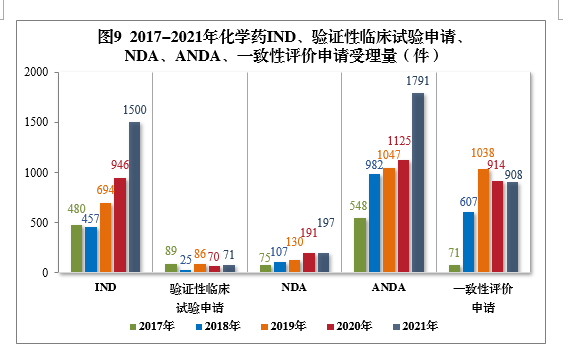
2021年需技术审评的化学药各类别注册申请受理量详见图8。2017-2021年化学药IND、验证性临床试验申请、NDA、ANDA、一致性评价申请受理量详见图9。
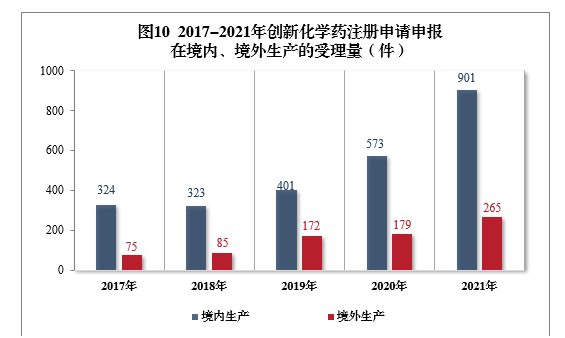
需技术审评的创新化学药注册申请共1166件(508个品种)11中,以生产场地类别统计,901件(385个品种)申报在境内生产,265件(123个品种)申报在境外生产。2017-2021年创新化学药注册申请申报在境内、境外生产的受理量详见图10。
(五)需技术审评的生物制品注册申请受理情况
2021年受理需技术审评的生物制品注册申请1999件,其中,预防用生物制品注册申请229件、治疗用生物制品注册申请1755件和体外诊断试剂15件。以注册申请类别统计:
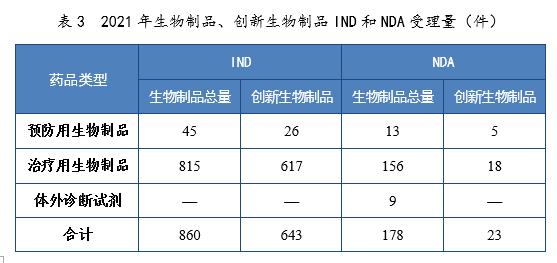
IND 860件,同比增长48.28%,包括创新生物制品IND 643件(423个品种),同比增长131.29%。其中,预防用生物制品IND 45件,包括创新预防用生物制品IND 26件(16个品种),治疗用生物制品IND 815件,包括创新治疗用生物制品IND 617件(407个品种)。
NDA 178件,同比增长41.27%,包括创新生物制品NDA 23件(16个品种),同比增长27.78%。其中,预防用生物制品NDA 13件,包括创新预防用生物制品NDA 5件(2个品种);治疗用生物制品NDA 156件,包括创新治疗用生物制品18件(14个品种);体外诊断试剂9件。
补充申请916件。境外生产药品再注册申请45件。
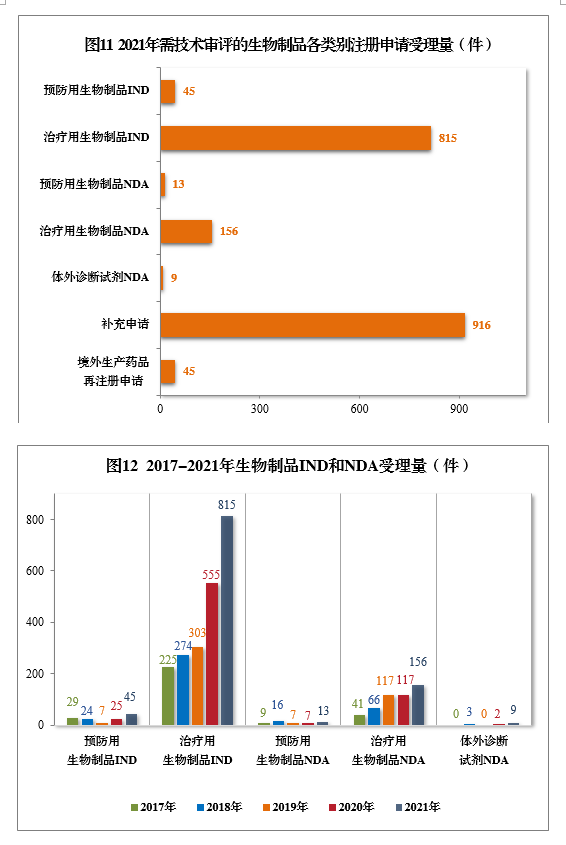
2021年生物制品、创新生物制品IND和NDA受理量详见表3。2021年需技术审评的生物制品各类别注册申请受理量详见图11。2017-2021年生物制品IND和NDA受理量详见图12。
表3 2021年生物制品、创新生物制品IND和NDA受理量(件)
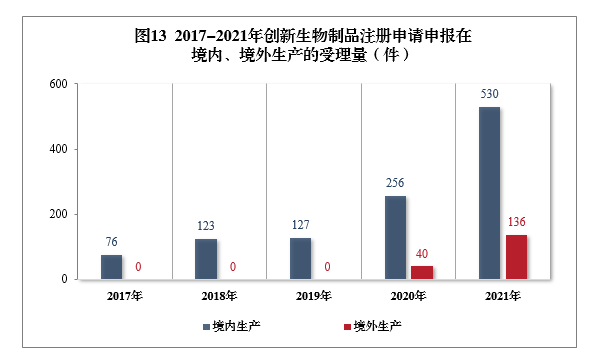
需技术审评的创新生物制品注册申请共666件(439个品种12)中,以生产场地类别统计,境内生产创新生物制品注册申请530件(354个品种),境外生产创新生物制品注册申请136件(85个品种)。2017-2021年创新生物制品注册申请申报在境内、境外生产的受理量详见图13。
(六)行政审批注册申请受理情况
1.总体情况
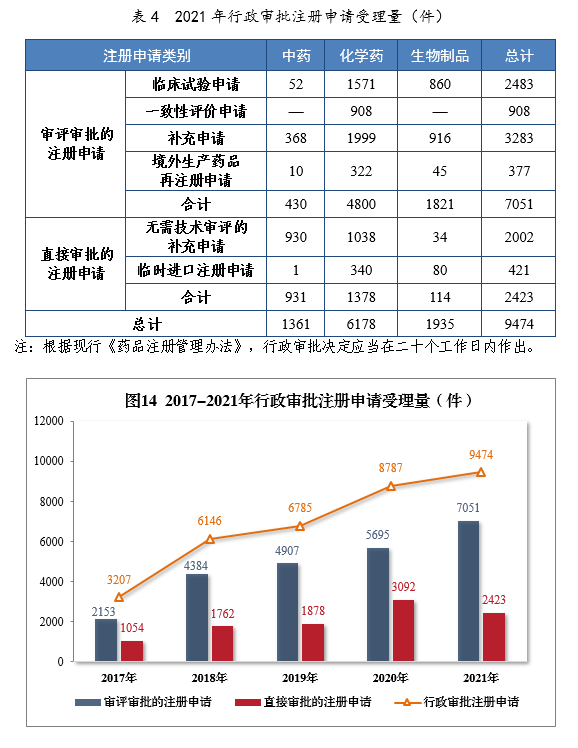
2021年受理行政审批注册申请9474件,同比增长7.82%。其中,直接审批的注册申请2423件;审评审批的注册申请137051件,同比增长23.81%,包括临床试验申请2483件,同比增长53.46%。
2021年行政审批注册申请受理量详见表4。201714-2021年行政审批注册申请受理量详见图14。
2.审评审批的注册申请受理情况
2021年受理审评审批的注册申请7051件,以药品类型统计,中药注册申请430件,同比增长40.07%;化学药注册申请4800件,同比增长17.50%,占全部审评审批的注册申请受理量的68.08%;生物制品注册申请1821件,同比增长39.75%。
以注册申请类别统计,临床试验申请2483件,同比增长53.46%;一致性评价申请908件;补充申请3283件,同比增长16.13%;境外生产药品再注册申请377件,同比增长14.94%。
3.直接审批的注册申请受理情况
2021年受理直接审批的注册申请2423件,以药品类型统计,中药注册申请931件、化学药注册申请1378件、生物制品注册申请114件。以注册申请类别统计,补充申请2002件、临时进口注册申请421件。
第二章 药品注册申请审评审批情况
(一)总体情况
1.全年审评审批工作情况
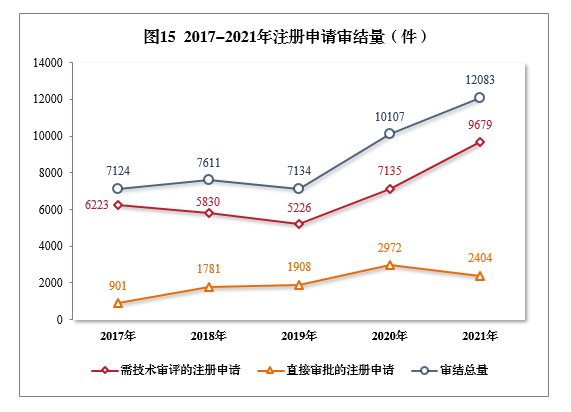
2021年审结的15注册申请共12083件16,同比增长19.55%。
审结的需技术审评的注册申请9679件,同比增长35.66%,包括技术审评的注册申请2632件,审评审批的注册申请7039件,药械组合注册申请8件。
审结直接审批的注册申请2404件。2017-2021年注册申请审结量详见图15。
截至2021年底,有5652件注册申请正在审评审批中;待申请人回复补充资料1353件。根据56号公告,2021年审结原料药注册申请494件。截至2021年底,有1302件原料药注册申请正在审评审批中;待申请人回复补充资料582件。
2.需技术审评的各类注册申请审结情况
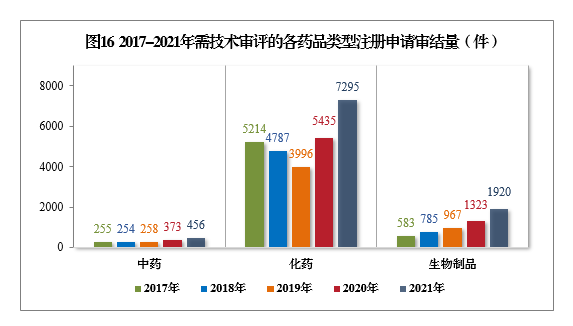
2021年审结的需技术审评的9671件17注册申请中,以药品类型统计,中药注册申请456件,同比增长22.25%;化学药注册申请7295件,同比增长34.22%,占全部需技术审评审结量的75.43%;生物制品注册申请1920件,同比增长45.12%。
2017-2021年需技术审评的各药品类型注册申请审结量详见图16。
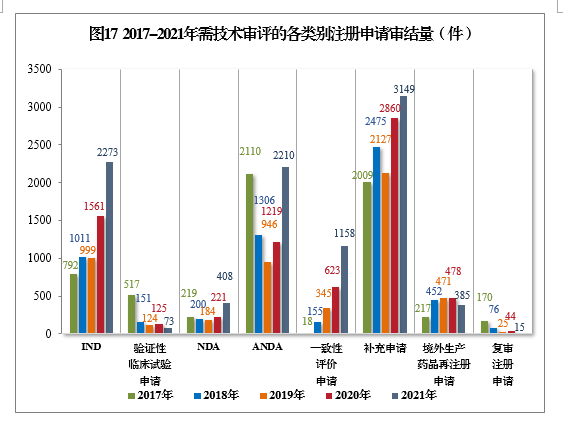
以注册申请类别统计,IND 2273件,同比增长45.61%;NDA 408件,同比增长84.62%;ANDA 2210件,同比增长81.30%;一致性评价申请1158件,同比增长85.87%;补充申请3149件,同比增长10.10%。2017-2021年需技术审评的各类别注册申请审结量详见图17。
3.批准/建议批准情况
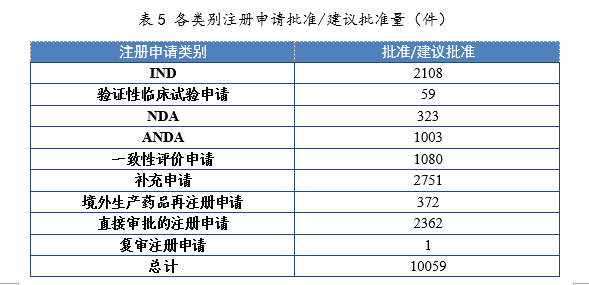
2021年批准IND 2108件,同比增长46.90%;建议批准NDA 323件(见附件1),同比增长55.29%;建议批准ANDA 1003件,同比增长9.26%;批准一致性评价申请1080件,同比增长87.18%。各类别注册申请批准/建议批准量详见表5。
建议批准境外生产原研药1876个品种(含新增适应症品种,见附件2)。
临床急需境外新药81个品种19中,截至2021年底,已有54个品种提出注册申请,51个品种获批上市,按审评时限审结率(以下简称按时限审结率)100%,临床急需境外新药审评审批情况见附件3。
4.各类别注册申请按时限审结情况
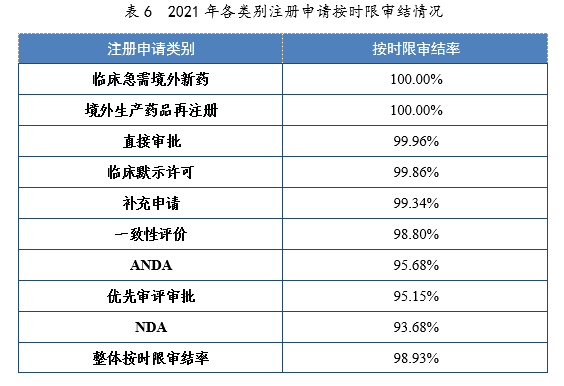
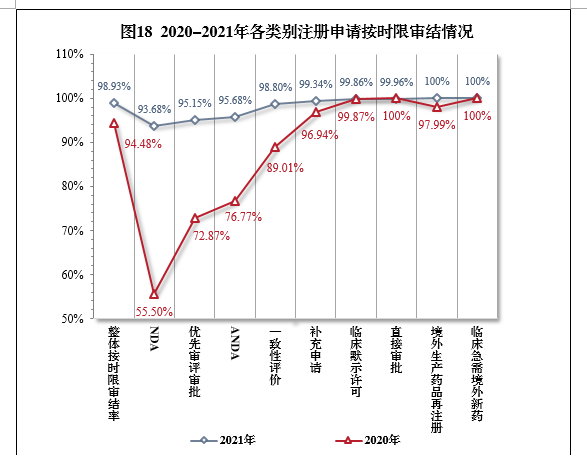
2021年,药审中心持续优化审评流程、严格审评时限管理、加快审评速度、强化项目督导,全年整体按时限审结率98.93%。其中NDA、ANDA、纳入优先审评审批程序的注册申请按时限审结率均超过90%,取得历史性突破。2021年各类别注册申请按时限审结情况详见表6,2020-2021年各类别注册申请按时限审结情况详见图18。
(二)创新药注册申请审结情况
1.总体情况
2021年审结创新药20注册申请1744件(943个品种),同比增长67.85%。
以药品类型统计,创新中药55件(55个品种),同比增长52.78%;创新化学药1085件(484个品种),同比增长45.44%;创新生物制品604件(404个品种),同比增长135.02%。
以注册申请类别统计,IND 1663件(885个品种),同比增长67.14%;NDA 81件(58个品种),同比增长84.09%。
2.批准/建议批准情况
2021年批准/建议批准创新药注册申请1628件(878个品种),同比增长67.32%。
以药品类型统计,创新中药39件(39个品种),同比增长39.29%;创新化学药1029件(463个品种),同比增长44.32%;创新生物制品560件(376个品种),同比增长141.38%。以注册申请类别统计,IND 1559件(831个品种),同比增长65.32%,NDA 69件(47个品种,见附件4),同比增长130.00%。
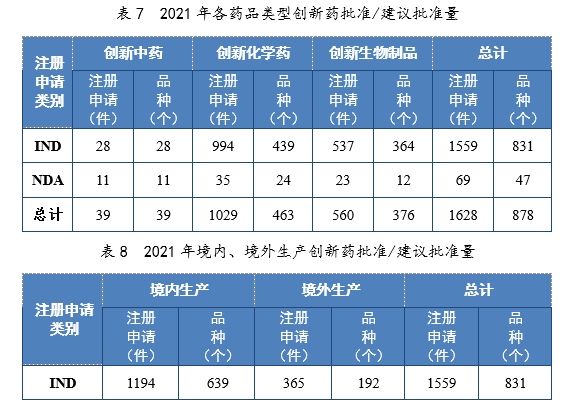
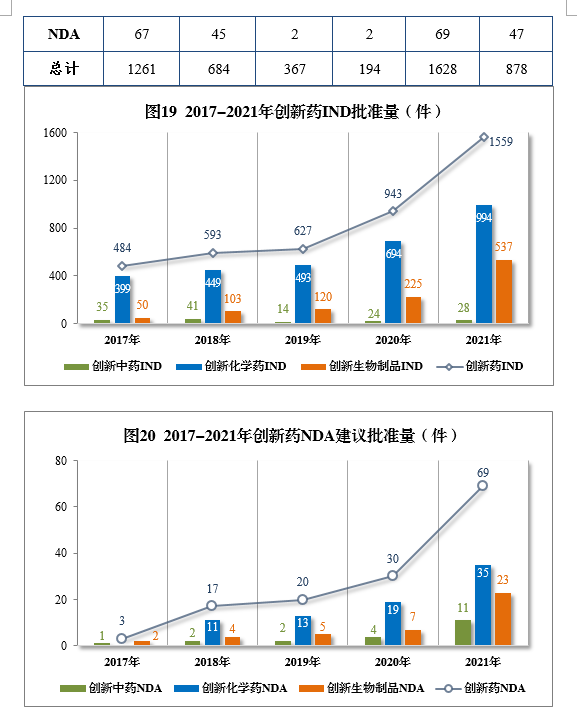
以生产场地类别统计,境内生产创新药1261件(684个品种),同比增长60.84%;境外生产创新药367件(194个品种),同比增长94.18%。2021年各药品类型创新药批准/建议批准量详见表7,2021年境内、境外生产创新药批准/建议批准量详见表8,2017-2021年创新药IND批准量详见图19,2017-2021年创新药NDA建议批准量详见图20。
(三)需技术审评的中药注册申请审结情况
1.总体情况
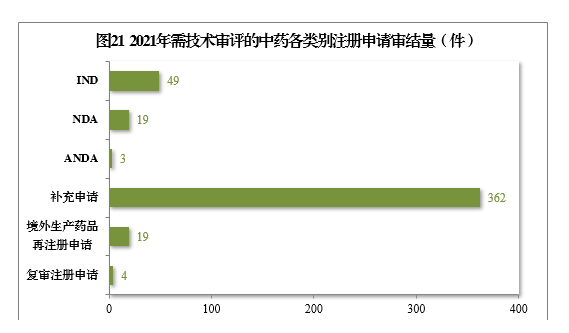
2021年审结需技术审评的中药注册申请456件,同比增长22.25%。以注册申请类别统计,IND 49件,同比增长32.43%;NDA 19件,同比增长216.67%;ANDA 3件。2021年需技术审评的中药各类别注册申请审结量详见图21。
2.批准/建议批准情况
2021年审结的中药IND中,批准34件,不批准9件。审结的中药NDA中,建议批准14件,建议不批准3件。2021年需技术审评的中药注册申请审结情况详见表9。
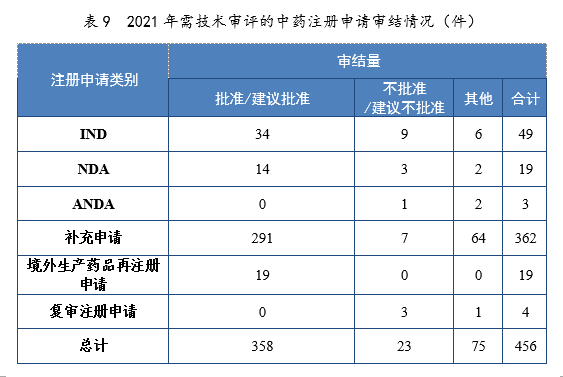
注:“其他”是指申请人未按规定缴纳费用、撤回申请等原因导致审评审批终止的情形。
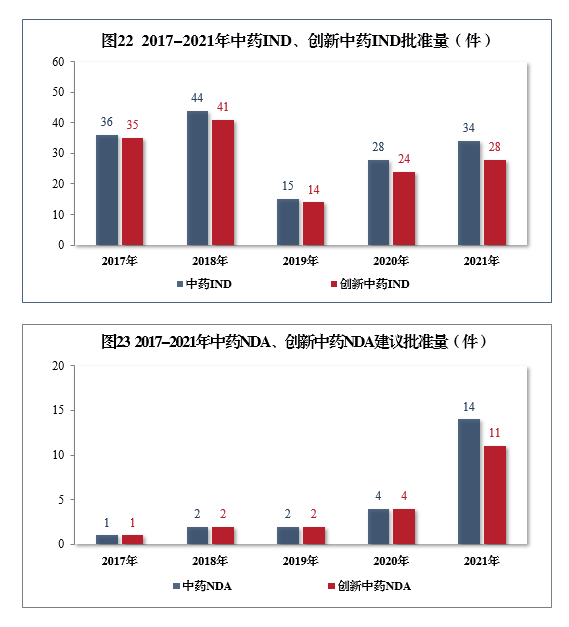
批准中药IND 34件,同比增长21.43%,包括创新中药IND 28件(28个品种),同比增长16.67%;建议批准中药NDA 14件,同比增长250.00%,创5年以来新高,包括创新中药NDA 11件(11个品种),同比增长175.00%。2017-2021年中药IND、创新中药IND批准量详见图22,2017-2021年中药NDA、创新中药NDA建议批准量详见图23。
批准的34件中药IND中,涉及13个适应症领域,其中消化8件、呼吸6件、妇科4件,共占52.94%,2021年批准中药IND的适应症领域分布量详见图24。
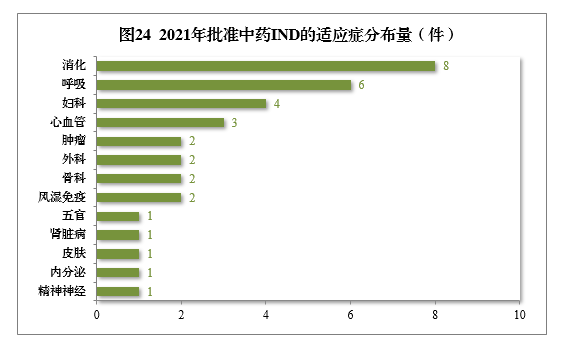
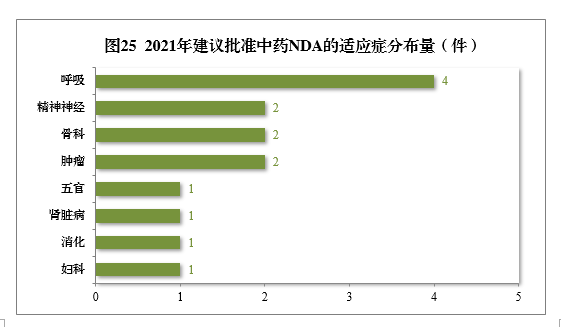
建议批准的中药NDA 14件中,呼吸肿瘤、精神神经、骨科药物较多,占全部中NDA批准量的71.43%。
2021年建议批准中药NDA的适应症分布量详见图25。
(四)需技术审评的化学药注册申请审结情况
1.总体情况
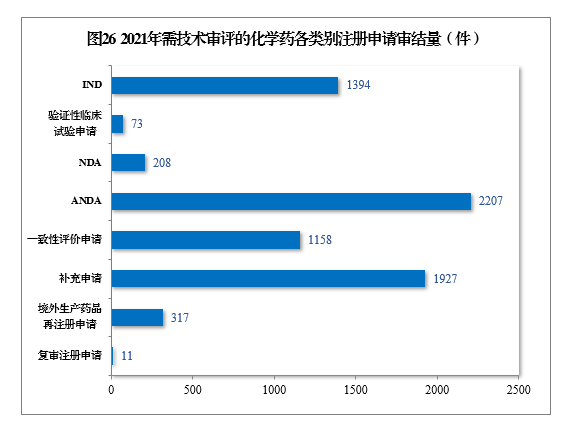
2021年审结需技术审评的化学药注册申请7295件。以注册申请类别统计,化学药临床试验申请1467件,同比增长35.21%;化学药NDA 208件,同比增长67.74%;化学药ANDA 2207件,同比增长81.50%;化学药一致性评价申请1158件,同比增长85.87%。2021年需技术审评的化学药各类别注册申请审结量详见图26。
2.批准/建议批准情况
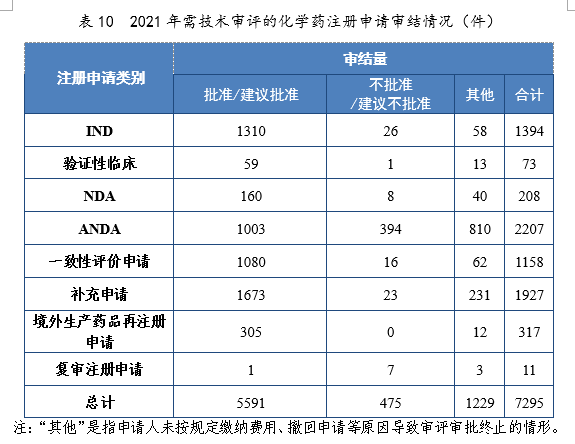
2021年审结的化学药IND中,批准1310件,不批准26件。审结的化学药NDA中,建议批准160件,建议不批准8件。审结的化学药ANDA中,建议批准1003件,建议不批准394件。2021年需技术审评的化学药注册申请审结情况详见表10。
批准化学药IND 1310件,同比增长44.43%,其中创新化学药IND 994件(439个品种),同比增长43.23%。2017-2021年化学药IND、创新化学药IND批准量详见图27。
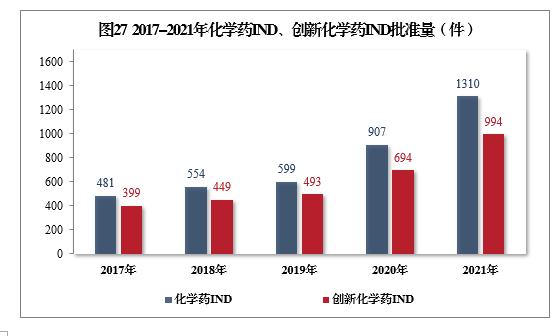
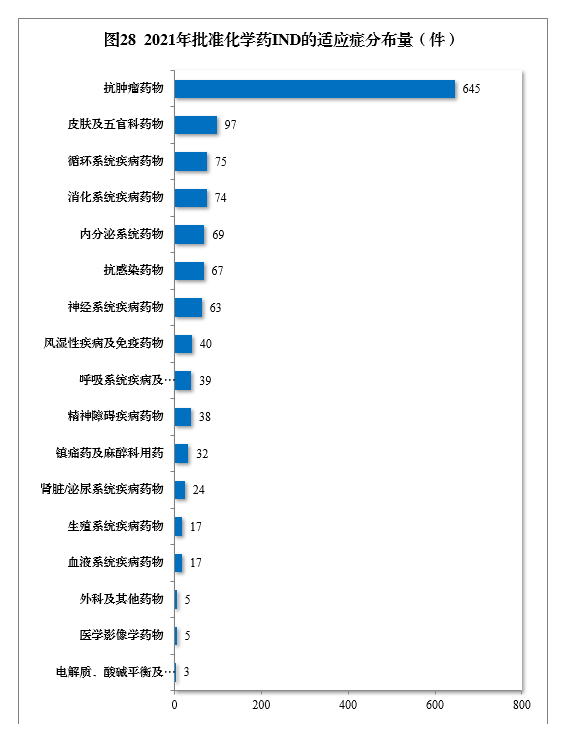
批准的化学药IND 1310件中,抗肿瘤药物、皮肤及五官科药物、循环系统疾病药物、消化系统疾病药物、内分泌系统药物、抗感染药物和神经系统疾病药物较多,占全部化学药IND批准量的83.21%。2021年批准化学药IND的适应症分布量详见图28。
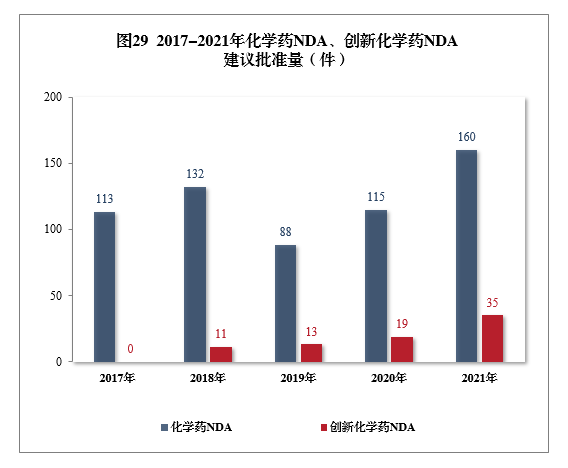
建议批准化学药NDA 160件,同比增长39.13%,包括创新化学药35件(24个品种),同比增长84.21%;建议批准化学药ANDA 1003件,同比增长9.26%。2017-2021年化学药NDA、创新化学药NDA建议批准量详见图29。
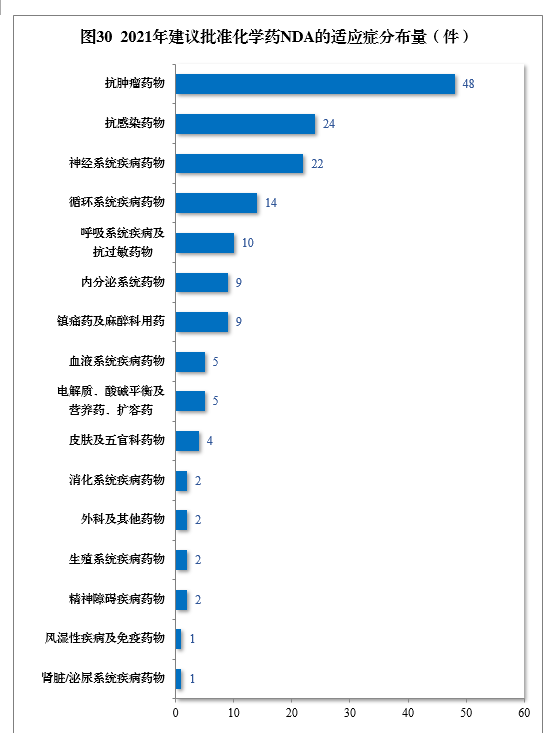
建议批准的化学药NDA 160件中,抗肿瘤药物、抗感染药物、神经系统疾病药物、循环系统疾病药物、呼吸系统疾病及抗过敏药物药物较多,占全部化学药NDA批准量的73.75%。2021年建议批准化学药NDA的适应症分布量详见图30。
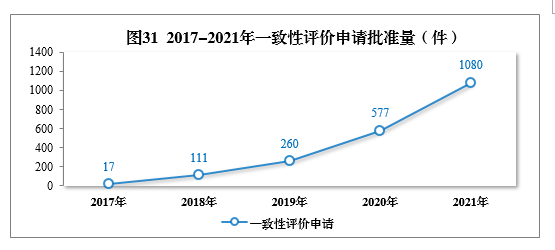
审结一致性评价申请共1158件,批准1080件。其中口服固体制剂一致性评价申请391件,注射剂一致性评价申请689件,2017-2021年一致性评价申请批准量详见图31。2021年批准的一致性评价品种见附件5。
 微信公众号
微信公众号
